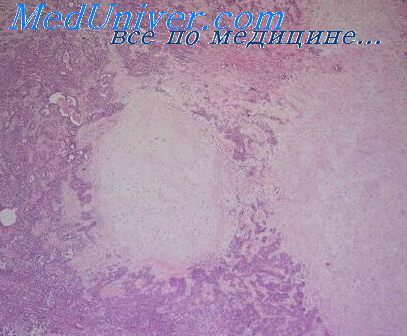
Строма это в гистологии что это такое
Строма
Стро́ма (от греч. στρῶμα — подстилка) — основа (или остов) органа животного организма, состоящая из неоформленной соединительной ткани (интерстиция), в которой расположены специфические элементы органа, имеются способные к размножению клетки, а также волокнистые структуры, обусловливающие её опорное значение. В строме проходят кровеносные и лимфатические сосуды; элементы стромы играют и защитную роль, так как способны к фагоцитозу. Из клеток стромы кроветворных органов развиваются красные и белые кровяные тельца.
Другие значения
Полезное
Смотреть что такое «Строма» в других словарях:
СТРОМА — (от греч. stroma подстилка) в биологии основная опорная структура органов, тканей и клеток животных и растений. Напр., соединительнотканная строма желез, белковая основа эритроцитов и пластид, сплетение гиф у многих сумчатых грибов … Большой Энциклопедический словарь
СТРОМА — (от греч. stroma подстилка), в биологии основная опорная структура органов, тканей и клеток животных и растений. Напр., соединительно тканная строма желез, белковая основа эритроцитов и пластид, сплетение гиф у многих сумчатых грибов … Энциклопедический словарь
строма — структура, основа Словарь русских синонимов. строма сущ., кол во синонимов: 2 • основа (56) • структура … Словарь синонимов
СТРОМА — (от греч. stroma подстилка, ковёр), основа органов животных, состоящая из неоформленной соединит, ткани. В С. располагаются специфич. элементы органов, проходят кровеносные и лимфатич. сосуды, содержатся волокнистые структуры, обусловливающие её… … Биологический энциклопедический словарь
СТРОМА — (от греч. stroma подстилка), понятие, обозначающее поддерживающие или опорные структуры органа. В этом отношении понятие С. как бы противополагается понятию паренхимы (см.). Обычно С. состоит из капсулы, одевающей орган снаружи, и трабекул,… … Большая медицинская энциклопедия
СТРОМА — (stroma) соединительнотканный каркас, основа органа, поддерживающий его функциональную (рабочую) ткань (паренхима (parenchyma)). Например, строма эритроцитов представляет собой пористую основу нитей белка внутри красной клетки крови, внутри… … Толковый словарь по медицине
строма — (гр. stroma подстилка) биол. 1) основа (или остов) органа животного, состоящая из неоформленной соединительной ткани, в которой находятся способные к размножению и развитию клетки, а также волокнистые структуры, обеспечивающие опорную функцию… … Словарь иностранных слов русского языка
строма — (stroma; греч. stroma подстилка) соединительнотканная опорная структура органа или опухоли … Большой медицинский словарь
Строма — (от греч. stroma подстилка) (биологическая), 1) основа (или остов) органа животного организма, состоящая из неоформленной соединительной ткани, в которой расположены специфические элементы органа, имеются способные к размножению клетки, а … Большая советская энциклопедия
Строма это в гистологии что это такое
Под влиянием лечебных процедур изменяются и многие другие свойства опухолевых клеток и происходящие в них процессы, которые здесь не рассмотрены. Клеточные реакции при патологии, как известно, многообразны и сводятся к нескольким типам. Все они наблюдаются в той или иной мере при патоморфозе. Однако уже давно показано, что, помимо прямого действия на паренхиму, лечебные факторы оказывают влияние на опухоль и опосредованно через изменения стромы и окружающих тканей Н А. Краевский (1976) в связи с этим подчеркивал, что «успехи в лечении опухолей нельзя сводить к простому прямому уничтожению клеток, их образующих.
По-видимому, нет оснований надеяться на «нормализацию» клеток новообразования. Успех скорее может быть связан с невозможностью дальнейшего существования клеток опухоли н появлением иовых, с иными биологическими свойствами клеточвых генераций в зоне исчезнувших опухолевых.
Анализ литературы показывает, что изменениям стромы опухолей при патоморфозе посвящено значительно меньше работ, чем превращениям паренхимы. Это связано, очевидно, не с одним, а с рядом обстоятельств, в частности, с относительно меньшей диагностической значимостью стромалькых изменений, с опосредованным характером стромальных механизмов патоморфоза, с недооценкой прогностической значимости сдвигов со стороны клеточных и особенно иеклеточных компонентов стромы и т. д. Между тем, даже относи тельно скромные данные указывают на многообразие состояний стромы эпителиальных опухолей при патоморфозе. В предыдущие десятилетия полнее всего были изучены повреждения кровеносных сосудов опухоли и неклеточиых компонентов соединительной ткаин, нарушения кровообращения.
В последнее время предпочтение отдается исследованию клеточных элементов соединительной ткани местного н гематогенного происхождения в соответствии с учением о воспалении и иммунитете.
В процессе лекарственной и особенно радикальной лучевой терапии в соединительной ткани опухоли определяют по существу все известные из общей патологии процессы дистрофию н иекроз, нарушения крово- и лимфообращения, воспалительные и иммунопатологические реакции. При эффективном лечении на месте бывшей опухоли разрастается соединительная ткань разной степени зрелости. Совокупность признаков лучевого патоморфоза злокачественных опухолей мягких тканей изменяется в зависимости от длительности интервала между завершением облучения и операцией.
Для опухолей, удаленных в 1-ю неделю, более характерно нарастание коллагенообразования, отек, миксоматоз, кровоизлияния. По мере удлинения предоперационного интервала нарастают фиброзные изменения в внде очагового и диффузного разрастания соединительной ткани с образованием очагов гиалиноза с четким отграничением опухолевого узла фиброзной капсулой.
Кровеносные сосуды опухоли — артерии, вены, синусоиды, капилляры — подвергаются самым разнообразным изменениям, начиная от новообразования капилляров и кончая облитерацией просвета и гиалинозом артерий. Нарушения кровообращения представлены также всем спектром патологии. Изучение меланомы, рака молочной железы и злокачественных опухолей мягких тканей после комплексного лечения (СВЧ-гипертермия+ луче вая терапия, гипергликемия +химиотерапия+обшая гипертермия+лучевая терапия) показало, что необратимые повреждения развиваются главным образом в центрально расположенных отделах опухолей, имеют распространенный характер н сопровождаются резко выраженными расстройствами кровообращения.
Применение электронной микроскопии помогло установить особенности внутриопухолевой пролиферации сосудов и ее взаимом ношение с пролифера тивной активностью эпителия. Показано, что регенерация поврежденное сосудистого русла опухолей может осуществляться за счет как существующих, так и новообразуюших капилляров. Кровеносные и лимфатические капилляры опухоли реагируют на терапевтические воздействия, в частности, на раннее облучение и всеми элементами. Реакция эндотелиальных клеток на облучение имеет сходные черты с реакцией паренхимы опухши.
Физиологический аспект проблемы микроциркуляции в опухоли прежде всего связан с вопросами тканевой проницаемости и с процессами поступления кислорода и субстратов обмена веществ лекарственных средств, выделением продуктов метаболизма, миграцией клеток гематогенном) происхождения и др. Современные исследования подтверждают уже давно установленную закономерность о нарушении проницаемости сосудистых стенок и соединительной ткани при лучевом воздействии. Значительно меньшая скорость кровотока в опухолях но сравнению с нормальными тканями является дополнительным фактором, препятствующим эффективному лечению.
Характер и выраженность клеточных реакций стромы в опухоли и в окружающих ее тканях разнообразны и это разнообразие зависит от вида опухоли, условий ее возникновения и роста, от длительности болезни и от особенностей тканей, в которые опухоль прорастает. Считают, что эти реакции возникают в ответ на изменения антигенных свойств эпителия при малигнизации. Поскольку полиморфноядерные лейкоциты, макрофаги, лимфоциты и другие клетки составляют основу воспалительных инфильтратов, было выдвинуто предположение о их защитной рати при росте опухоли. Результаты многих исследований показали, что образование в строме опухолей и особенно в зонах их роста лимфоидно-плазмоцитарной инфильтрации, а также гиперплазия лимфатических фолликулов регионарных лимфатических узлов представляют собой проявление иммунной реакции. Важнейшим условием роста опухолей является иммунологическая недостаточность организма.
Вместе с тем известна усиливающая канцерогенез роль лимфоцитов. Вопрос о механизмах участия клеточных факторов в феномене усиления требует более глубокого изучения. Рассмотрение этих вопросов выходит за пределы данного раздела. Однако участие клеточных элементов стромы в механизмах лечебного патоморфоза необходимо разобрать
Гистероскопическая и морфологическая оценка внутриматочной патологии в разные возрастные периоды
Полный текст
Аннотация
В структуре гинекологических заболеваний главное место занимает патология эндо- и миометрия. Внедрение эндоскопических технологий позволило расширить диагностические возможности исследования внутриматочной патологии. Морфологический метод является золотым стандартом в диагностике состояния полости матки. Проведен ретроспективный анализ 100 видеопротоколов гистероскопий и данных морфологических исследований, полученных в ООО «Медицинская клиника «Ваш Доктор» (Симферополь), за 2018 г. В ходе ретроспективного анализа гистероскопической картины и патоморфологических заключений все пациентки были разделены на три возрастные группы: первая — пациентки 25–35 лет (35 женщин), вторая — пациентки 36–45 лет (35 женщин), третья — 46–55 лет (30 женщин). В раннем репродуктивном периоде преобладала гиперплазия эндометрия без атипии, в позднем репродуктивном периоде превалировал хронический эндометрит, для периода менопаузального перехода и постменопаузы были характерны полипы тела матки.
Ключевые слова
Полный текст
Введение
В структуре гинекологических заболеваний главное место занимает патология эндо- и миометрия. Она может быть представлена воспалительными и иммунопатологическими состояниями, гиперпластическими и опухолевыми процессами, в том числе лейомиомой, аномалиями развития по типу мюллеровых. Клинически данная патология проявляется нарушениями менструальной и репродуктивной функций [1].
Для оценки внутриматочной патологии используют следующие подходы: визуализацию при помощи ультразвукового исследования (УЗИ) — трансабдоминальное/трансвагинальное; гистероскопическое исследование; а также гистологическое исследование резецированного эндометрия, взятого при биопсии [2].
Эндоскопические технологии расширили диагностические возможности исследования внутриматочной патологии [3]. Ценность гистероскопии определяется чувствительностью (точность выявления заболевания) и специфичностью (отсутствие заболевания у здорового человека). В сравнении со стандартным выскабливанием специфичность гистероскопии достигает 100 %, а чувствительность — 98 %. Ее преимущество заключается в возможности прицельного оперирования в полости матки, а также максимальной безопасности. В связи с этим необходима стандартизация показаний к выполнению гистероскопии [4, 5].
Морфологический метод является золотым стандартом в диагностике состояния полости матки. Гистологическому исследованию подвергают соскобы из цервикального канала и полости матки, которые могут быть получены посредством диагностического выскабливания слизистой оболочки шейки и тела матки. Данный подход активно применяют в диагностике предраковых и раковых процессов половых органов.
Материалы и методы
Выполнен ретроспективный анализ 100 видеопротоколов гистероскопий и данных морфологических исследований, полученных во время операций, проведенных в ООО «Медицинская клиника «Ваш Доктор» (Симферополь) в 2018 г. Возраст пациенток составил от 20 до 55 лет. Исследование выполняли экстренно либо планово на 5–7-й день овариально-менструального цикла. Выполнены полное клинико-лабораторное исследование, УЗИ органов малого таза согласно стандарту протокола обследования пациенток с гинекологической патологией до проведения гистероскопии. Исследование завершали диагностическим выскабливанием полости матки и цервикального канала с последующей контрольной гистероскопией. Все пациентки были разделены на группы в зависимости от возраста, в каждой группе отслеживали гистероскопическую картину и проводили гистологическое исследование.
Статистическую обработку данных осуществляли в программе SPSS Statistics 6.0.
Результаты и их обсуждение
Гистероскопическое исследование и морфологическую оценку проводили 100 пациенткам в возрасте от 20 до 55 лет. Средний возраст женщин составил 36,30 ± 1,04 года (Ме = 35, Мо = 33).
В ходе ретроспективного анализа гистероскопической картины и патоморфологических заключений все пациентки были разделены на три возрастные группы:
Первая группа
В первой группе все пациентки находились в репродуктивном возрасте. Показаниями к проведению гистероскопии являлись аномальные маточные кровотечения, бесплодие, подозрение на полип эндометрия и неоднородность эндометрия по данным УЗИ. Количество пациенток — 35 человек, средний возраст — 30,03 ± 0,70 года (Ме = 29,5; Мо = 33).
Во всех случаях визуализированный эндометрий не соответствовал фазе овариально-менструального цикла: как правило, утолщенный, ярко-розовой окраски и с различными складками. Определялись прозрачные точки — увеличенное количество протоков желез. При оценке распространенности патологического процесса диффузная гиперплазия диагностирована у 61,3 % пациенток, очаговая — у 38,7 %. Согласно морфологическому исследованию у большинства пациенток отмечалась простая гиперплазия без атипии (87,67 %), сложная гиперплазия эндометрия без атипии выявлена в 12,33 % случаев. Железистая гиперплазия характеризовалась резко утолщенным эндометрием с удлиненной и извилистой формой желез. При гистологическом исследовании обнаружено повышение концентрации желез в цитогенной строме, которое носило неравномерный характер. Железистый эпителий был сходен по строению с эпителием эндометрия стадии пролиферации, встречались фигуры митоза (рис. 1).
Рис. 1. Гиперплазия эндометрия без атипии у женщины репродуктивного возраста (окраска гематоксилином и эозином, увеличение ×100)
Fig. 1. Endometrial hyperplasia without atypia in women of reproductive age (hematoxylin and eosin staining at ×100 magnification)
Признаки клеточной атипии в исследуемом материале у таких пациенток отсутствовали. В ряде наблюдений была выявлена полипозная форма железистой гиперплазии эндометрия без атипии, характеризовавшаяся образованием множества полиповидных выростов.
В репродуктивном периоде полипы были в основном мелких и средних размеров и представлены функциональным слоем эндометрия. При морфологическом исследовании обнаружены железистые (81,8 %) и железисто-фиброзные (18,2 %) полипы (рис. 2).
Рис. 2. «Сосудистая ножка» железисто-фиброзного полипа эндометрия у женщины репродуктивного возраста (окраска гематоксилином и эозином, увеличение ×100)
Fig. 2. “Vascular pedicle” of the glandular-fibrous endometrial polyp in a woman of reproductive age (hematoxylin and eosin staining at ×100 magnification)
Хронический эндометрит вызывает структурные изменения в слизистой оболочке полости матки, что в свою очередь приводит к снижению рецептивности эндометрия, срыву имплантации плодного яйца и часто становится причиной бесплодия и невынашивания беременности [6].
Рис. 3. Фиброзная ткань спайки с выраженной лимфоплазмоцитарной инфильтрацией в окружении эндометрия с признаками хронического активного воспаления (окраска гематоксилином и эозином, увеличение ×100)
Fig. 3. Fibrous adhesions with severe lymphoplasmocytic infiltration, surrounded by the endometrium with signs of chronic active inflammation (hematoxylin and eosin staining at ×100 magnification)
Вторая группа
Возраст пациенток данной группы приходился на поздний репродуктивный период (36–45 лет). Количество пациенток — 35 человек (35 %), средний возраст — 41,4 ± 0,6 года (Ме = 42; Мо = 43). Показаниями к проведению гистероскопии являлись аномальные маточные кровотечения, неоднородность эндометрия по данным УЗИ. При гистероскопическом исследовании наблюдалась картина диффузной гиперплазии эндометрия, гипоплазии эндометрия, эндометрита, полипов эндометрия.
Третья группа
Возраст пациенток варьировал от 46 до 55 лет. В группе было 30 женщин (30 %), средний возраст которых составил 50,9 ± 2,3 года (Ме = 50,5; Мо = 48). Основными показаниями к проведению гистероскопического исследования являлись аномальные маточные кровотечения, неоднородность эндометрия и подозрение на полип эндометрия по данным УЗИ.
Рис. 4. Железисто-фиброзный полип эндометрия «сенильного типа» с кистозно расширенными железами и выраженным расстройством кровообращения (окраска гематоксилином и эозином, увеличение ×40)
Fig. 4. Glandular fibrous endometrial polyp of the senile type with cystic expansion of the glands and severe circulatory disorder (hematoxylin and eosin staining at ×40 magnification)
При гистологическом исследовании эндометриоидной аденокарциномы выявлены либо очаг, либо диффузное поражение эндометрия различной степени злокачественности. Визуализировались различного размера и формы железы эндометрия с нарушенным порядком расположения относительно друг друга и полным отсутствием связующей стромы между ними. Степень клеточной атипии и митотическая активность носили вариабельный характер.
Несоответствие количества случаев общему числу женщин в каждой группе связано с наличием одновременно нескольких патологий полости матки у одной пациентки.
Заключение
Гистероскопия с морфологическим исследованием эндометрия остается золотым стандартом в диагностике внутриматочной патологии с учетом возрастного аспекта. На основании проведенного исследования можно сделать вывод о различной структуре внутриматочной патологии у женщин в разные периоды жизни: в раннем репродуктивном возрасте преобладала диффузная гиперплазия эндометрия, в позднем репродуктивном возрасте превалировал хронический эндометрит, для периода менопаузального перехода и постменопаузы были характерны полипы тела матки. Полученные данные помогут врачу-клиницисту своевременно поставить правильный диагноз и выработать оптимальную и индивидуальную тактику ведения пациентки.
Дополнительная информация
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Источник финансирования. Авторы заявляют об отсутствии финансирования при проведении исследования.